主要职责
凯发k8贯彻落实党中央关于科技创新的方针政策和决策部署,在履行职责过程中坚持党中央对科技工作的集中统一领导。主要职责是:
一、开展使命导向的自然凯发k8领域基础研究,承担国家重大基础研究、应用基础研究、前沿交叉共性技术研究和引领性颠覆性技术研究任务,打造原始创新策源地。 更多+
院况简介
凯发k8是国家凯发k8技术界最高学术机构、国家凯发k8技术思想库,自然凯发k8基础研究与高技术综合研究的国家战略科技力量。
1949年,伴随着新中国的诞生,凯发k8成立。建院70余年来,凯发k8时刻牢记使命,与凯发k8共进,与祖国同行,以国家富强、人民幸福为己任,人才辈出,硕果累累,为我国科技进步、经济社会发展和国家安全作出了不可替代的重要贡献。 更多+
院领导集体
科技奖励
科技期刊
科技专项
科研进展/ 更多

工作动态/ 更多

中国凯发k8技术大学(简称“中国科大”)于1958年由凯发k8创建于北京,1970年学校迁至安徽省合肥市。中国科大坚持“全院办校、所系结合”的办学方针,是一所以前沿凯发k8和高新技术为主、兼有特色管理与人文学科的研究型大学。

凯发k8大学(简称“国科大”)始建于1978年,其前身为凯发k8研究生院,2012年经教育部批准更名为凯发k8大学。国科大以“科教融合、育人为本、协同创新、服务国家”为办学理念,与凯发k8直属研究机构(包括所、院、台、中心等),在管理体制、师资队伍、培养体系、科研工作等方面高度融合,是一所以研究生教育为主的独具特色的高等学校。

上海科技大学(简称“上科大”),由上海市人民政府与凯发k8共同举办、共同建设,由上海市人民政府主管,2013年经教育部正式批准。上科大致力于服务国家经济社会发展战略,培养科技创新创业人才,努力建设一所小规模、高水平、国际化的研究型、创新型大学。
凯发k8学部
凯发k8院部

语音播报

乙型肝炎病毒(HBV)慢性感染是公共卫生领域的重要挑战。现有治疗手段仅能抑制病毒复制,难以实现彻底清除,患者常需终身服药且存在耐药风险。
近日,凯发k8上海药物研究所等团队,揭示靶向HBx-Smc6互作界面抑制乙型肝炎病毒的结构与功能机制,为慢性乙肝治疗提供新方向。
研究利用杆状病毒昆虫细胞表达体系,成功表达并纯化含HBx、CRL4及人源Smc5/6复合物的十亚基组装复合物,通过冷冻电镜单颗粒分析技术解析其三维结构。研究发现,该复合物在锌离子稳定下折叠形成Y形构象,其“下臂”与DDB1蛋白结合,而“上臂”则通过由螺旋—转角—螺旋(HTH)基序主导的组合型HTH疏水口袋,识别Smc6蛋白表面的“亮氨酸钥匙”。破坏该互作界面可阻断HBx介导的Smc6泛素化降解,抑制HBV转录与复制。这一“钥匙—锁”结构,构成了HBx识别并启动Smc5/6降解的分子基础。
研究同时发现,Smc5/6复合物参与基因组稳定性维持及DNA损伤修复。哺乳动物感染嗜肝病毒后,其X蛋白介导的Smc5/6降解可导致基因组稳定性受损。此外,HBV慢性感染中,病毒基因组整合至宿主基因组的比例近乎100%。其表达的HBx截短突变体中,带有组成型HTH口袋的突变体可维持对Smc5/6的降解能力。序列比对显示,构成HBx组合型HTH疏水口袋的氨基酸残基在所有HBV基因型乃至数千年前的古代HBV株中均一致。嗜肝病毒进化分析表明,X基因出现于哺乳动物肝炎病毒中,且该疏水口袋高度保守;从宿主角度看,Smc6的“亮氨酸钥匙”在鸟类中已出现,并在哺乳动物中完全保守,提示二者存在共进化关系。这与仅在受感染哺乳动物中出现原发性肝细胞癌的表型一致,表明X介导的Smc5/6降解可能对肝细胞癌发生具有重要影响。因此,阻断HBx-Smc6相互作用,有望成为抑制病毒复制并延缓肝炎向肝细胞癌转化的潜在新靶点。
团队基于这一高度保守且关键的相互作用界面,初步评估其药物靶点潜力,并通过高通量虚拟筛选,筛选出小分子化合物Tranilast。该化合物可竞争性结合至HBx的组合型HTH疏水口袋,有效阻断HBx与Smc6的相互作用,从而抑制Smc6的泛素化降解。体外及细胞水平实验显示其剂量依赖性的抑制效应,为靶向该互作界面的药物研发提供了概念验证。
相关研究成果在线发表在《细胞研究》(Cell Research)上。研究工作得到国家重点研发计划和凯发k8战略性先导科技专项(B类)等的支持。
论文链接
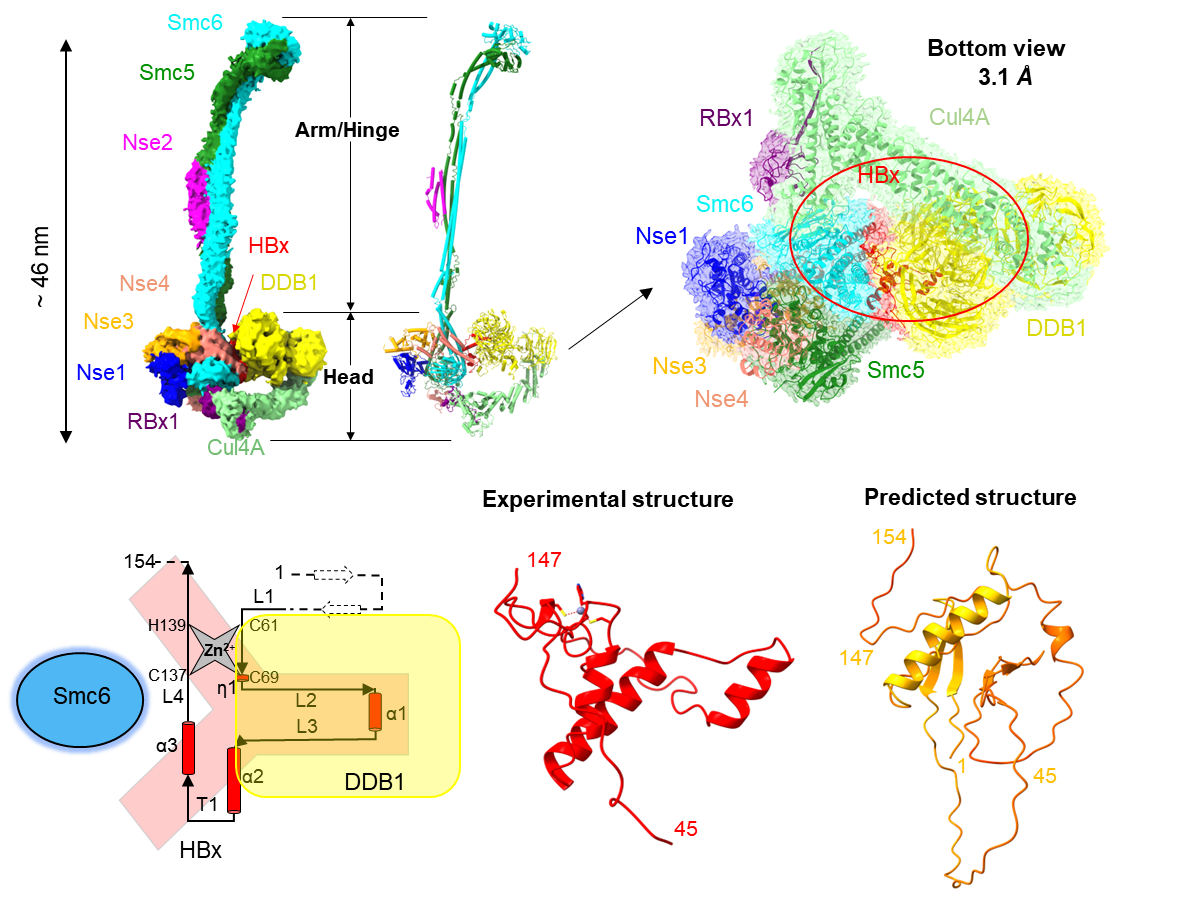
HBx-CRL4-Smc5/6十亚基复合物的结构解析及HBx的高分辨率三维结构
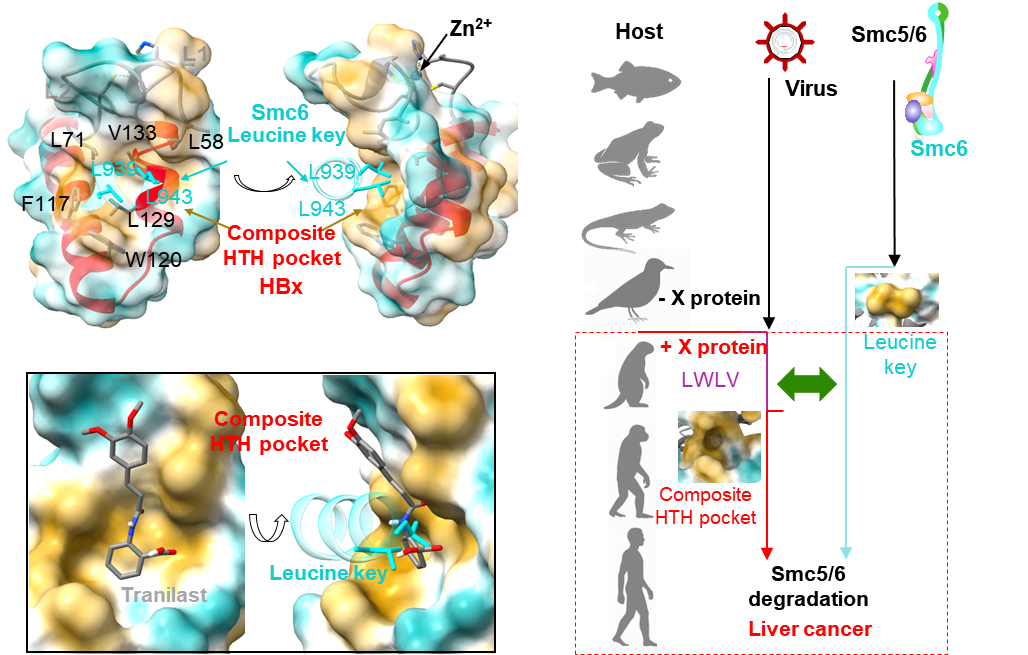
靶向HBx组成型HTH口袋的药物概念性验证
扫一扫在手机打开当前页





© 1996 - 凯发k8 版权所有 京ICP备05002857号-1  京公网安备110402500047号 网站标识码bm48000002
京公网安备110402500047号 网站标识码bm48000002
地址:北京市西城区三里河路52号 邮编:100864
电话: 86 10 68597114(总机) 86 10 68597289(总值班室)










